4. Gaser
Aggregationstillstånd
4.1 Förbränning
●
●
En kemisk reaktion mellan ett ämne och
syre.
Fullständig förbränning (om syre finns i
överskott), t.ex. etanol + syre
C2H6OH (l) +3O2 (g) → 3H2O (g) + 2CO2
(g)
●
Om det finns för lite syre blir
förbränningen ofullständig och giftig
kolmonoxid (CO) bildas.
4.2 Gaser
●
Den luft vi andas består av:
Idealgasmodellen
Gasens tryck, p
●
Kraft per ytenhet av kärlet.
●
Enhet: pascal, Pa
(använd N m-2 i beräkningarna)
●
Normalt lufttryck: 101,325 kPa
Gasens volym, V
●
●
En gas fyller alltid helt och hållet ett kärl och gasens
volymen är därför alltid samma som kärlets volym.
Enhet: m3 (dm3)
Gasens temperatur, T
●
Enhet: kelvin, K
Boyles lag
●
PV = k
volymen av en gas är omvänt proportionell mot dess
tryck.
Charles lag
●
V = k3 T
Volymen av en gas är direkt proportionell mot dess
temperatur.
Gay-Lussac's lag
●
P = k 2T
Temperaturen av en gas är direkt proportionell mot
dess tryck.
Avogadro´s lag
●
●
●
Vid samma tryck och temperatur
innehåller lika stora volymer av vilken gas
som helst samma antal partiklar (=samma
substansmängder).
Vid normalt tryck och temperatur, NTP
(273 K och 101,3 kPa) har en mol gas
volymen 22,4 dm3.
Molvolymen för en ideal gas vid NTP:
22,41 dm3/mol
Gasernas allmänna tillståndsekvation
p = gasens tryck
V = gasens volym
n = gasens substansmängd
R = den allmänna gaskonstanten 8,31451 J K-1 mol-1
T = gasens temperatur
Läxa
●
Läs. s. 84-89 i boken
+ uppgifterna på utdelade pappret
●
(Uppg. 79 s. 94)
Ex. Trinitrotoluen (TNT) är ett av de vanligaste sprängämnena. Vid
en explosion sönderfaller det till kolmonoxid, väte,kväve och kol
enligt:
C7H5N3O6 (s) → CO (g) + H2 (g) + N2 (g) + C(s)
a) Bestäm koefficienterna för reaktionslikheten.
b) Hur många gram TNT exploderade, då det bildades
2,76 liter gasfasprodukter (NTP)?
5. Energiförändringar i kemiska reaktioner
5.1 Reaktioner och energi
●
●
I kemiska reaktioner binds eller frigörs det energi.
Att bryta bindningar kräver energi, medan energi friges
då bindningar bildas.
5.2 Energityper i kemiska reaktioner
●
●
●
Då värmeenergi tillförs börjar partiklarna röra sig fortare i
slumpmässig riktning.
Värme: Den totala mängden energi i en given mängd
substans (är beroende av mängden substans).
Temperatur: Ett medeltal av de enskilda partiklarnas
kinetiska energi ett ämne (är oberoende av mängden
substans).
Båda bägarna har
samma temperatur, men
den med 1l innehåller
dubbelt så mycket värme
jämfört med den med
500 ml.
Entalpi, H
●
Entalpi: Värmeinnehållet hos en substans “värme inuti”.
Entalpiförändring, kJ
●
●
Det är omöjligt att mäta den
verkliga entalpin hos
utgångsämnen och
produkter, men däremot kan
entalpiförändringen (ΔH) för
en reaktion mätas.
Förändring i värmeinnehåll
mäts med en kalorimeter.
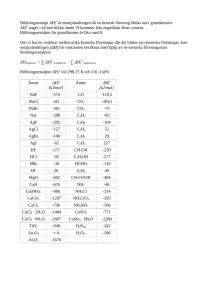
5.4 Reaktionsentalpi, ΔHº (kJ/mol)
●
●
Den värme som binds (+) eller frigörs (-) i en kemisk
reaktion.
Referenstillstånd: 298,15 K och 101,325 kPa
5.4.1 Exoterm reaktion
●
Energi frigörs.
●
Produkterna är stabilare än reaktanterna.
känns varm
Exoterma reaktioner:
- förbränning
- neutralisation
Exoterma processer:
- stelning (l → s)
- kondensation (g → l)
- sublimering (g → s)
5.4.2. Endoterm reaktion
●
Värme binds.
●
Produkterna är mindre stabila än utgångsämnena.
Känns kall
Endoterma reaktioner:
- fotosyntes
Endoterma processer:
- smältning (s → l)
- sublimering (s → g)
- förångning (l → g)
Läxa
●
Läs s. 100-102, 108-109
●
Uppg. 102, 103 s. 139.
●
●
Exoterm reaktion: bindningarna i produkterna är
starkare än i utgångsämnena (= produkterna har lägre
energi och överloppsenergin avges).
Endoterm reaktion: bindningarna i utgångsämnena är
starkare än i produkterna (= produkterna har högre
energi och extra energi måste tillföras).
Demo 1
Mg (s) + 2HCl (aq) → Mg2+ (aq)+ 2 Cl- (aq) + H2 (g)
Demo 2
NH4NO3 (s) → NH4+ (aq) + NO3- (aq)
5.3 Energin hos byggstenarna i ett ämne
Mikro- och makronivå
Byggstenarna i ett ämne
(atomer, joner, molekyler)
●
Egenskaper som kan iakttas
och mätas
Då man tillför värme ökar partiklarnas rörelseenergi.
●
Byggstenarna i ett ämne har:
–
Potentiell energi lagrad i bindningar (= kemisk
energi)
–
Rörelseenergi (ökar då man tillför värme)
Vattnets entalpi
●
●
Då is smälter brister endast en
del av vätebindningarna
mellan vattenmolekylerna.
Då vatten förångas brister alla
återstående vätebindningar.
Att förånga vatten kräver
mycket energi = förångningen
binder mycket energi (vatten
används därför till att släcka
bränder.
https://www.youtube.com/watch?v=CDTZoFGmZoc
http://www.youtube.com/watch?v=PcoiLAsUvq
Vattnets aggregationstillståndsentalpi
s. 111
En revesibel (omvänd)
process är exoterm (-) i ena
riktningen och endoterm (+) i
andra riktningen.
●
Ångbildningsentalpin för
vatten är +40.7 kJ/mol (100ºC)
och vattnets
kondenseringsvärme är då
-40.7 kJ/mol.
●
Smältentalpin för vatten är +
6.01 kJ/mol (0ºC) och vattnets
kristallisationsvärme -6.01
kJ/mol.
●
s. 114 ex. 2
●
5.5 Bildningsentalpi , ΔH Of
●
Reaktionsentalpin då 1 mol av en bestämd substans i
grundtillstånd bildas från sina grundämnen i
grundtillstånd.
Ag(s) + ½ Br2(l) → 1 AgBr(s) ∆Hf = -99.5 kJ mol-1
●
Vid bildning av den mest stabila formen av ett
grudämne är bildningsentalpin noll.
O2 (g) → O2 (g)
∆HfƟ =
0 kJ mol-1
Beräkning av reaktionsentalpi med hjälp av
bildningsentalpi
●
●
Om man känner till utgångssubstansernas och
produkternas bildningsentalpier kan man beräkna
reaktionsentalpin för vilken reaktion som helst.
Ex. Beräkna reaktionsentalpin för förbränning av
metan:
5.6 Bindningsenergi (kJ/mol)
●
●
Den mängd energi som behövs för att bryta ned 1 mol
av en kovalent bindning i gasfas.
Ju större bindningsenergi, desto starkare bindning.
H2 (g) →
2H (g)
ΔHϴ =
+ 436 kJ mol-1
Förbränning av metan
●
●
Vid förbränning har utgångssubstanserna lägre energi
än produkterna.
Överloppeenergin friges i form av ljus och värme.
Läxa
●
s. 140 uppg. 106, 111, 122
●
Läs s. 104-111, 120-121
Hess lag:
●
●
Entalpiförändringen i en kemisk
reaktion är oberoende av vilka
mellansteg reaktionen har.
Om en reaktion består av flera
mellansteg, är den totala
entalpiförändringen lika med summan
av ΔH för alla enskilda steg.
ΔH1 = ΔH2 + ΔH3 + ΔH4
ΔH1
ΔH2
ΔH4
ΔH3
Läxa
●
Läs s. 112-120
●
Uppg. 123, 131
5.8 Reaktionshastighet
●
Snabba och långsamma reaktioner
●
Reaktionshastighet:
- förändring i substansmängd (eller koncentration) hos ett
reagerande ämne under en bestämd tid ELLER
- förändring i substansmängd (eller koncentration) hos
reaktionsprodukter under en bestämd tid
H2 (g) + I2 (g) → 2HI (g)
Hastighetsfördelningen hos partiklar
Aktiveringsenergi, Ea
●
Den lägsta kinetiska energi som utgånssubstanserna i en
reaktion måste ha för att en kemisk reaktion skall kunna
ske.
Övergångstillstånd:
ett instabilt momentant tillstånd där gamla bindningar är delvis
upplösta och nya bindningar håller på att bildas.
Kollisionsteori
●
För att en reaktion skall kunna måste partiklarna:
–
kollidera med varandra i lämplig riktning
–
ha högre energi än aktiveringsenergin då de
kolliderar
Temperaturens inverkan på
reaktionshastigheten
●
Då partiklar (i gas, vätska eller fast form) upphettas:
- rör de sig snabbare och kolliderar oftare
- en större andel av de kolliderande partiklarna har
tillräcklig kinetisk energi för att åstadkomma en reaktion.
Koncentration
●
Antalet kollisioner mellan byggstenar
tilltar då koncentrationen i en
reaktionsblandning ökar.
Zn + 2 HCl → ZnCl2 + H2
Tryck
●
Ifall en eller flera av reaktanterna är gaser, tvingar ett
högre tryck partiklarna närmare varandra
(=”koncentrationen” ökar).
Partikelstorlek
●
●
Ifall utgångsämnet är fast sker reaktionen på ytan.
Reaktionshastigheten är snabbare för ett finfördelat
ämne.
CaCO3 (s) + 2HCl (aq) → CaCl2 + H2O (l) + CO2 (g)
Katalysator
●
En katalysator är ett ämne som försnabbar en kemisk
reaktion utan att själv förbrukas i reaktionen.
Läxa
●
Läs s. 130-138
●
s.145 uppg. 135
●
s.146 uppg. 138
Till provförberedelsen 27.3 kl 13.45-15
●
Gör alla uppgifter på de utdelade uppgiftspappren:
- KE03 Övningsuppgifter Kap3
- PROV I KE03
31.03.2014 (förra årets kursprov)
- Studentexamensuppgifter 20.3.2015 uppg.2,7,8 c) och d)
Till provet 30.3.2015
●
Läs boken kap. 1-5 (inte blåa rutorna och endast det vi
gått igenom under lektionerna)
●
Anteckningarna (s.1-15)
●
+ Utdelade uppgiftspapper
Provet består av:
●
En definitionsuppgift
●
Reaktionsformler a) balansera
b) hur många gram produkt bildas
c) begränsande reagens
d) utbyte
●
●
●
PV = nRT Hur stor volym gas bildas
Organiska reaktionstyper (Rita strukturformler för
reaktanter ELLER produkter)
Beräkna reaktionsentalpin m.h.a a) bindningsenergier
b) bildningsentalpier
●
Addera ihop reaktionslikheter och reaktionsentalpier
●
Entalpidiagram